Virus hémorragique de Crimée-Congo – Résultats de biologie structurale pour de futurs vaccins et traitements
La fièvre hémorragique de Crimée-Congo (FHCC) tient son nom d’une première description de cette maladie en Crimée en 1944, chez des militaires soviétiques, puis au Congo en 1956. Transmise à l’Homme par piqûre de tique ou contact direct avec des sécrétions d’animal ou de personne infectés, elle est mortelle dans 10 à 40% des cas.
Une équipe internationale de chercheurs apporte de nouvelles informations sur la structure d'anticorps dirigés contre le virus de la FHCC et le mécanisme de protection contre ce virus. Leurs résultats, basés sur des expériences menées dans trois synchrotrons, l’APS (USA), l’ESRF (Grenoble) et SOLEIL sur la ligne PROXIMA-2A, sont publiés dans la revue Science.
Chez la personne infectée, la FHCC provoque d’abord fièvre, maux de tête, douleurs musculaires puis la deuxième phase, hémorragique, est mortelle dans 10 à 40% des cas. L'OMS dispose actuellement d'une liste de 10 maladies prioritaires pour la recherche et le développement dans des contextes d'urgence. Sur cette liste figure le virus de la FHCC, qui est endémique en Europe de l'Est, en Asie, en Afrique et au Moyen-Orient. Toutefois, le réchauffement climatique ayant un impact sur les habitats des animaux et les schémas migratoires, ce virus pourrait s'infiltrer dans de nouvelles régions où il n'existait pas auparavant. On pense que des cas récents en Espagne, en Italie et au Royaume-Uni seraient dus à des tiques transportées par des oiseaux. Ainsi, la FHCC représente une menace substantielle de passer d'une endémie régionale à la prochaine pandémie mondiale.
Or, la structure des anticorps dirigés contre le virus de la FHCC et le mécanisme mis en place par l'organisme pour neutraliser ce virus sont encore mal connus, ce qui constitue un obstacle important à la mise au point de traitements médicaux et de vaccins susceptibles de sauver des vies dans les communautés où le virus est endémique.
On sait que le virus de la FHCC infecte les cellules hôtes par l'intermédiaire de ses glycoprotéines Gc et Gn, qui subissent des changements de conformation quand il fusionne avec la membrane de la cellule hôte. Par contre, la façon dont les anticorps les plus puissants contre le virus, appelés ADI-36121 et ADI-37801, neutralisent le VFHCC restait inconnue.
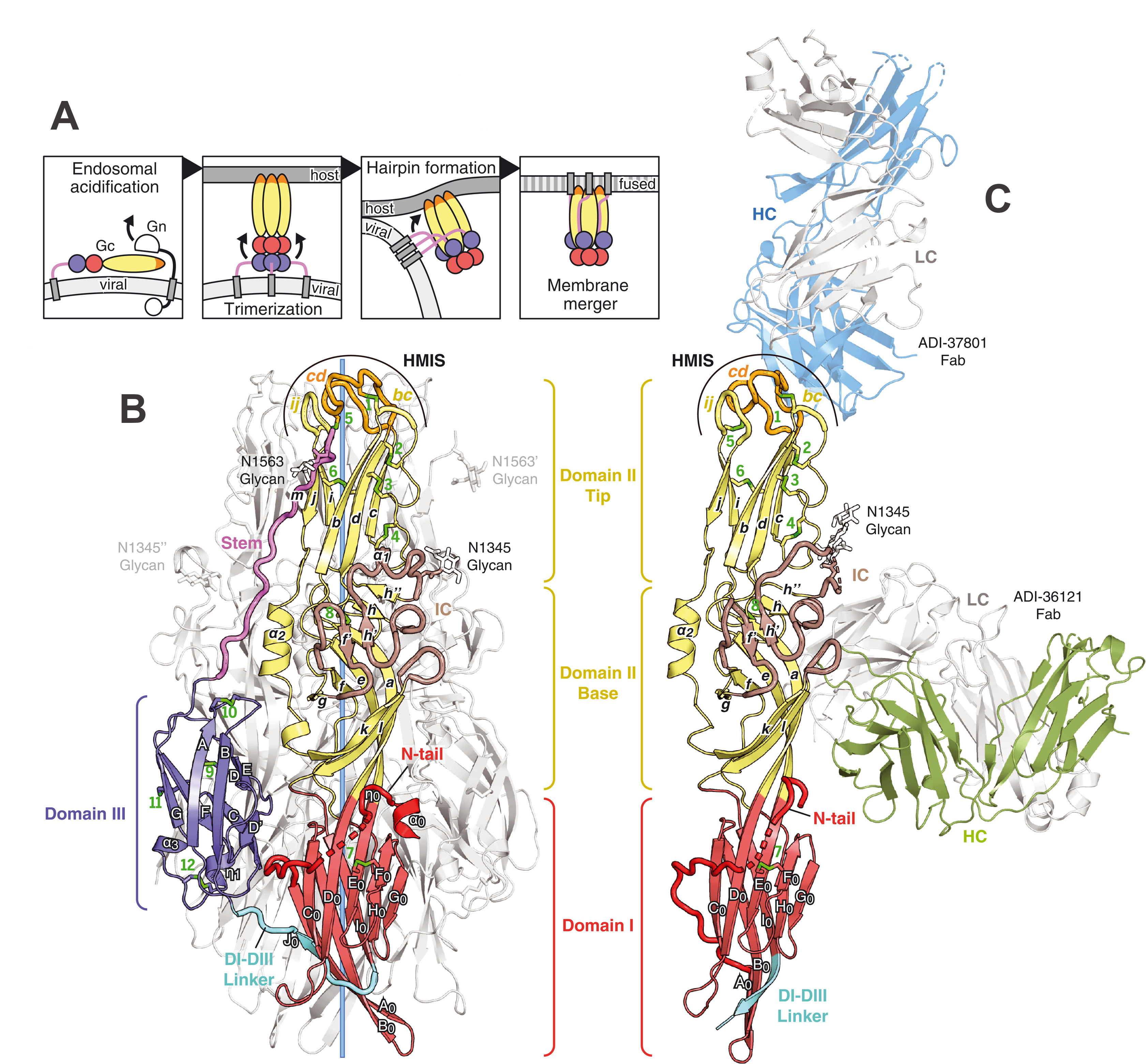
Grâce aux données de diffraction des rayons X obtenues sur les lignes de lumière 19-ID du Centre de biologie structurelle de l'APS, ID23-1 de l'ESRF et PROXIMA-2A de SOLEIL, l’équipe de scientifiques a pu obtenir la structure 3D de la protéine Gc post-fusion et de la protéine Gc pré-fusion liée aux fragments de liaison des anticorps ADI-36121 et ADI-37801 , voir figure 1 : la structure 3D du trimère de protéine Gc virale post-fusion (fig 1B) a été obtenue grâce à des mesures de diffraction des rayons X réalisées à l’ESRF (ligne ID23-1) et à SOLEIL (ligne PROXIMA-2A) ; la structure de la protéine virale en complexe avec le fragment d’anticorps (fig 1C) a été obtenue grâce à des mesures de diffraction des rayons X réalisées à l’APS (ligne 19-ID-D).
Les résultats montrent clairement que les deux anticorps agissent en synergie pour empêcher la fusion membranaire induite par la protéine Gc, en bloquant les changements de conformation des glycoprotéines.
Bien que d'autres connaissances soient nécessaires pour mettre au point des traitements et des vaccins permettant de limiter et de prévenir la propagation du virus de la FHCC, cette étude fournit des informations fondamentales nécessaires à la découverte et au développement de vaccins. Ce virus étant déjà endémique dans le monde entier et compte tenu de son impact important sur la vie humaine, certaines sociétés pharmaceutiques, comme Moderna, sont actuellement en train d’étudier des vaccins en vue d'essais cliniques.