Restauration et conservation d’objets archéologiques ferreux
La préservation des objets métalliques issus de fouilles archéologiques nécessite des traitements de stabilisation, tels que les traitements de déchloruration, classiquement mis en œuvre dans les ateliers de restauration.
Les mécanismes de déchloruration d’objets archéologiques ferreux ont été mis en évidence par observation directe in situ de la transformation des produits de corrosion, en utilisant notamment la diffraction des rayons X sur la ligne DIFFABS.
Altération des objets en milieu marin
L’étude physico-chimique de lingots de fer mis au jour lors de fouilles archéologiques d’une épave gallo-romaine (Ier siècle avant J.-C.) au large des Saintes-Maries-de-la-Mer a mis en évidence des produits de corrosion contenant du chlore : l’akaganeite β-FeO1-x(OH)1+xClx et un hydroxychlorure de fer β-Fe2(OH)3Cl, phase particulièrement instable en milieu oxydant. En effet, les phases qui se forment lors des processus de corrosion du fer au sein de différents milieux (marin, terrestre ou atmosphérique), peuvent fixer certains sels du milieu, dont les chlorures. Après les fouilles, s'ils ne sont pas rapidement stabilisés, les objets subissent fréquemment de nouveaux processus de corrosion dus notamment à la présence de l'oxygène de l'air. Il s’en suit alors une dégradation souvent rapide et inéluctable des couches de corrosion par fissuration, provoquant la perte d’objets centenaires uniques et irremplaçables.
Déchlorurer pour stabiliser
Des traitements de déchloruration sont classiquement mis en œuvre dans les ateliers de restauration afin de stabiliser les objets issus de fouilles archéologiques (marines notamment). L’évaluation de l’efficacité de ces traitements, leur optimisation ou le développement de nouveaux protocoles font partie des préoccupations quotidiennes des professionnels en charge de la protection de ces objets du patrimoine. La connaissance fine des transformations subies par ces objets lors de traitements de déchloruration apporterait une meilleure compréhension permettant de répondre à ces préoccupations avec une plus grande justesse.
Le processus révélé
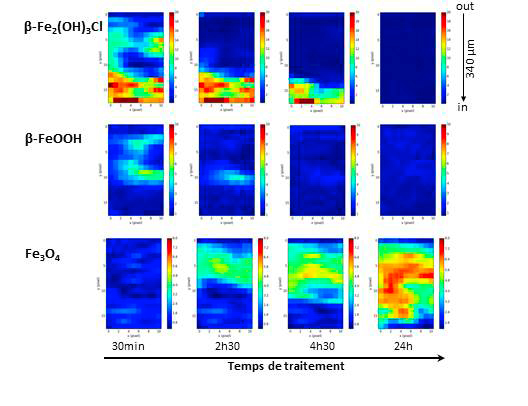
Afin d’identifier in situ les phases obtenues par la transformation des produits de corrosion au cours du processus de déchloruration, une cellule chimique spécifique a été conçue. Cette dernière contient un échantillon issu d’une barre de fer, donc constitué de métal et de produits de corrosion, ainsi que, circulant à la surface des produits de corrosion, une solution chimique de soude (NaOH), aérée ou désaérée. Le suivi in situ de l'évolution structurale du système de corrosion est effectué sur la ligne de lumière DIFFABS : des cartographies de diffraction des rayons X sous micro-faisceau révèlent la distribution des différents produits de corrosion à l’échelle micrométrique et leur transformation au cours du traitement.
Le système de corrosion initial résultant des processus de corrosion du fer en milieu marin se révèle être principalement constitué d’hydroxychlorure de fer β-Fe2(OH)3Cl. Il est constaté que cette phase est rapidement dissoute par la solution chimique alcaline de traitement. Des produits de corrosion plus ou moins stables se forment, tels que la magnétite Fe3O4 et l’hydroxyde ferreux Fe(OH)2, et ce quelle que soit la teneur en oxygène de la solution de traitement. En revanche, en solution aérée, la précipitation d’un composé de transition surnommé « rouille verte », hydroxysel à valence mixte du fer FeII3FeIII(OH)8Cl, 2H2O, est localement observé. Ce produit, extrêmement instable, est présent uniquement au cours du processus en solution, car transformé en d’autres produits de corrosion à la fin de l’expérimentation. Ce composé peut se transformer en akaganeite, impliquant un danger potentiel quant à la réelle stabilisation de l’objet traité, puisque cela implique qu’un résidu de phase chlorée reste dans la couche. Au contraire, l’utilisation d’une solution désaérée conduit à la formation de produits de corrosion bien plus stables et évite la formation de composés intermédiaires et résiduels contenant du chlore ; ces derniers pouvant potentiellement participer à des reprises de corrosion inattendues.
Cette étude a mis en évidence les processus réels des traitements de stabilisation sur des objets en fer en vue de les optimiser en maitrisant des paramètres tels que l’aération de la solution de traitement. La conclusion de cette étude conduit à préconiser, dans la mesure du possible au sein des ateliers de restauration, de stabiliser les objets en utilisant un milieu de traitement désaéré, et ceci afin d’assurer la conservation du métal et donc des collections sur le long terme.