Un catalyseur moléculaire capable de former des liaisons carbone-carbone à partir de CO2
Le dioxyde de carbone (CO2) est un gaz à effet de serre naturel, dont la surproduction par l’Homme (par combustion des énergies fossiles notamment) contribue au réchauffement de la planète. Mais ce déchet industriel est aussi une opportunité économique potentielle : le CO2 peut être utilisé pour fabriquer des produits chimiques essentiels en s’affranchissant du pétrole, ou pour stocker sous forme de carburants l'énergie provenant de sources renouvelables et intermittentes.
Comment ? Grâce à des réactions électrochimiques nécessitant l’usage de catalyseurs.
Dans cette étude, un catalyseur moléculaire composé d’éléments chimiques abondants (C, N, H, Fe) a été utilisé pour réduire le CO2 en hydrocarbures légers par voie électrocatalytique. Les résultats montrent que ce catalyseur est capable de former des liaisons carbone-carbone, ouvrant la voie à des processus chimiques complexes.
La réduction électrocatalytique du CO2 est une technologie prometteuse pour la conversion de ce déchet industriel abondant en produits chimiques de base ou en carburants. Les catalyseurs utilisés jusqu’à présent ne produisent que des composés à un seul carbone (C1) ou, dans le cas de catalyseurs contenant du cuivre, à deux carbones (C2). Malgré plusieurs décennies de recherche, le cuivre n’est pas efficace pour produire des composés possédant plus de deux liaisons carbone-carbone et le mécanisme de cette réaction est toujours débattu.
Par ailleurs, les catalyseurs moléculaires à base de macrocycles (molécules cycliques de grande taille) sont connus pour leur capacité à produire des composés de type C1, avec une très bonne sélectivité. Dans cette étude, les scientifiques de la ligne de lumière LUCIA ont exploré la capacité d’un de ces catalyseurs à produire des composés comportant deux ou plus liaisons C-C (C2+), afin de proposer de nouvelles stratégies pour l’optimisation de ces catalyseurs.
Formation inattendue de liaisons C-C
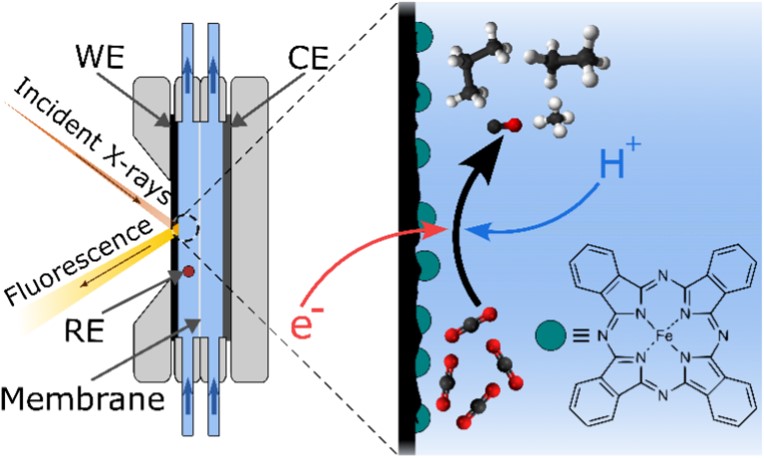
Afin de réaliser la réduction électrocatalytique du CO2, la phthalocyanine de fer (FePc) a été sélectionnée. Il s’agit d’un catalyseur disponible commercialement et uniquement composé d’éléments abondants : carbone, azote, hydrogène et fer. Ce catalyseur a été déposé sous la forme d’un film mince sur une électrode de carbone puis inséré dans une cellule d’électrolyse à circulation (voir figure 1), laquelle permet également de réaliser des expériences de spectroscopie d’absorption des rayons X au cours de la catalyse. Dans des conditions optimales, FePc produit du monoxyde de carbone (CO) à hauteur de 80%, complété par de l’hydrogène (H2) pour les 20% restants.
L’objectif initial était d’obtenir un maximum de CO. Mais une erreur de manipulation a conduit au dépôt d’une plus grande quantité de catalyseur sur l’électrode et à l’observation de produits inattendus.
En effet, l’analyse par chromatographie en phase gaz des produits volatiles a montré la présence d’hydrocarbures légers saturés et insaturés, tels que l’éthylène, l’éthane, le propylène, le propane, le butène et le butane. Ces composés comportent de deux à quatre atomes de carbone, ce qui implique la formation de liaisons carbone-carbone (C-C) au cours de la réaction catalytique.
Origine du carbone et stabilité du catalyseur
Les hydrocarbures obtenus au cours de la réaction le sont en très petites quantités (inférieures à 1%). De nombreuses expériences de contrôle ont été effectuées afin de s’assurer d’une part de l’origine des atomes de carbone et d’autre part de la stabilité du catalyseur. Des expériences réalisées en l’absence de CO2 (mais en présence de catalyseur) ou en l’absence de catalyseur (mais en présence de CO2) ne produisent aucun hydrocarbure, indiquant que le CO2 et le catalyseur sont deux éléments requis pour produire les composés de type C2+. Des mesures de chromatographie en phase gaz couplée à la spectrométrie de masse ont été réalisées en présence de CO2 marqué au carbone 13. Les résultats montrent de manière indubitable la formation des hydrocarbures à partir du 13CO2 – la source de carbone utilisée dans la réaction catalysée par la phthalocyanine de fer est donc bien le dioxyde de carbone.
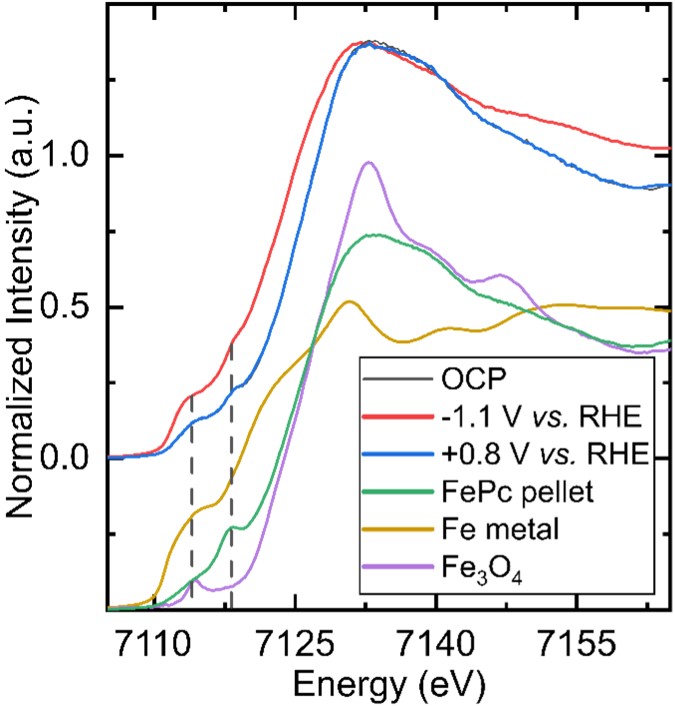
Par ailleurs, des expériences de spectroscopie d’absorption des rayons X réalisées durant la réaction de catalyse sur la ligne LUCIA du Synchrotron SOLEIL (voir figure 2), démontrent la stabilité du catalyseur au cours de la réaction.
Conclusion
L’étude des produits minoritaires obtenus au cours de la réduction électrocatalytique du CO2 par la phthalocyanine de fer a permis de montrer pour la première fois que ce composé est capable de former des hydrocarbures légers (C1 à C4) contenant jusqu’à trois liaisons C-C. Des mesures de spectroscopies infra-rouge et d’absorption des rayons X ont montré que le catalyseur conserve sa structure moléculaire intacte, durant et après la réaction catalytique. Ces observations ouvrent la porte à l’amélioration de cette famille de catalyseurs : leur structure chimique pourra être modifiée à façon pour optimiser la sélectivité vis-à-vis de ces hydrocarbures légers.