Un analogue de la vitamine D pour lutter contre le cancer avancé de la prostate
La vitamine D est connue pour ses activités anticancéreuses, notamment sur la progression du cancer de la prostate, mais son utilisation clinique reste limitée. Des scientifiques de l’Institut de Génétique et de Biologie Moléculaire et Cellulaire (IGBMC) ont démontré qu’un analogue de la vitamine D, conçu à partir de données structurales, présente une fenêtre thérapeutique¹ plus large que la vitamine D naturelle. Ils ont identifié le mécanisme précis responsable de l’activité anticancéreuse de cet analogue. En outre, ils ont montré que l’utilisation de cet analogue en combinaison avec le docétaxel, un agent chimiothérapeutique utilisé contre les cancers avancés de la prostate, permet de surmonter la chimiorésistance au docétaxel.
La ligne de lumière PROXIMA-2A de SOLEIL a contribué à ces résultats.
Le cancer de la prostate (PCa) est la troisième cause de décès par cancer chez les hommes. Les traitements de référence reposent sur la privation d’androgènes, mais ceux-ci induisent souvent un cancer de la prostate résistant à la castration, pour lequel le traitement de choix est le docétaxel. Cependant, l’efficacité de ce médicament est limitée car la plupart des patients développent une chimiorésistance.
La forme bioactive de la vitamine D (également appelée 1,25D3) exerce ses effets lorsqu’elle se lie à son récepteur nucléaire (VDR) : cette liaison induit l’activité de transcription d’ARN du récepteur VDR. Les protéines synthétisées suite à ces transcriptions interviennent dans la régulation de l’homéostasie du calcium et du phosphate, mais aussi la croissance et la différenciation cellulaires, l’anti-prolifération, l’apoptose et les réponses immunitaires innée et adaptative. L’interaction entre la vitamine D et le VDR joue ainsi un rôle clé pour ces différentes fonctions biologiques.
De faibles taux circulants de vitamine D, ainsi qu’une perturbation de l’activité transcriptionnelle du VDR, ont été associés à la progression du cancer de la prostate. Mais les doses thérapeutiques de vitamine D favorisent l’absorption du calcium, entraînant une hypercalcémie, c’est pourquoi il est nécessaire de disposer d’un analogue de la vitamine D ayant des propriétés anti-inflammatoires et/ou antiprolifératives sans cet effet sur l’absorption du calcium.
De nombreuses études précliniques ont montré un effet synergique du docétaxel associé à la vitamine D, mais les effets de la vitamine D sur la chimiorésistance dans le cancer de la prostate résistant à la castration restent inconnus. Les chercheurs de l’IGBMC ont caractérisé un nouvel analogue de la vitamine D et étudié son efficacité en association avec le docétaxel pour restaurer la sensibilité au traitement dans le cancer de la prostate avancé.
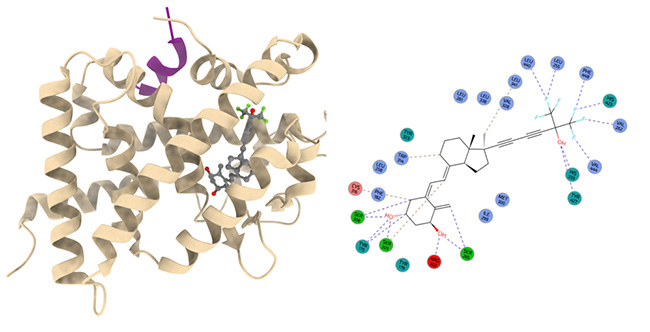
Plus de 4000 analogues de la vitamine D ont été synthétisés, et certains ont montré des activités anti-inflammatoires et/ou antiprolifératives puissantes in vitro, mais peu ont trouvé une application clinique. Les scientifiques de l’IGBMC ont conçu l’analogue Xe4MeCF3, qui comporte une chaîne latérale rigidifiée, un groupement méthyle sur l’atome de carbone C17, ainsi que deux groupements trifluorométhyle (figure 1). Ils ont utilisé la ligne de lumière PROXIMA-2A de SOLEIL pour déterminer la structure 3D du complexe VDR- Xe4MeCF3 et étudier son mode de liaison. La structure atomique du complexe a révélé des interactions supplémentaires, formées notamment entre le composé Xe4MeCF3 et l’hélice C-terminale du récepteur, dues à la fluorination des groupes méthyle terminaux de l’analogue. Les triples liaisons introduites pour verrouiller la conformation active de la chaîne latérale permettent un gain important de l’entropie dans la réaction de liaison, ce qui explique une activité transcriptionnelle accrue du récepteur.
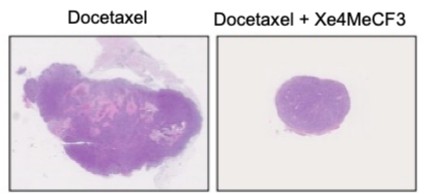
Les activités de Xe4MeCF3 ont été caractérisées, révélant que cet analogue est plus puissant que la vitamine D pour induire l’activité de transcription du VDR et qu’il possède une fenêtre thérapeutique plus large. Fait important, l’association Xe4MeCF3-docétaxel s’est révélée capable de freiner la croissance tumorale en induisant l’apoptose des cellules et en réduisant l’agressivité des cellules tumorales restantes (figure 2).
Les résultats de cette étude mettent en lumière des relations structure-fonction essentielles pour l’activité du VDR et révèlent le potentiel des agonistes du VDR pour surmonter la résistance au docétaxel dans les cancers de la prostate résistants à la castration, ouvrant ainsi de nouvelles perspectives pour la prise en charge clinique de cette maladie réfractaire à fort impact socio-économique.
¹ Fenêtre thérapeutique : plage de concentration d’un médicament permettant d’obtenir un effet thérapeutique efficace avec un minimum d’effets indésirables.