Recherche industrielle contre le cancer : des résultats, obtenus grâce à des données recueillies à SOLEIL, publiés dans la revue Nature
L’apoptose intrinsèque (mort cellulaire programmée) est une réponse aux lésions irréparables de l'ADN : si l’ADN de certaines cellules a subi de telles lésions, ces cellules sont alors marquées pour indiquer qu’elles doivent être détruites. Les cellules cancéreuses sont des cellules dont l'ADN est endommagé mais dans lesquelles existent des mécanismes qui leur permettent d'éviter l'apoptose. Par conséquent, elles continuent à proliférer même si elles ne fonctionnent pas normalement.
L'apoptose est régulée par une série de protéines dites BCL2, soit pro-apoptotiques soit anti-apoptotiques. Les protéines BCL2 pro-apoptotiques BAK et BAX ont pour fonction de s’accumuler pour former des canaux dans la membrane externe de la mitochondrie, permettant la libération de cytochrome C dans le cytoplasme. Le cytochrome C active alors des caspases (enzymes de contrôle qui interviennent dans l'apoptose en clivant, et donc désactivant, certaines protéines), ce qui va déclencher la mort cellulaire programmée. Dans les cellules saines, cette agrégation de BAK ou BAX pour former un canal est empêchée par des protéines anti-apoptotiques BCL2. Mais si la cellule est marquée pour être détruite, par exemple suite à une lésion irréparable de l'ADN, un autre ensemble de protéines BCL2 pro-apoptotiques produites par la cellule va bloquer les protéines BCL2 anti-apoptotiques dans le cytoplasme, favorisant de manière indirecte l'agrégation de BAX et BAK.
Dans de nombreux types de cancer (i.e. leucémie myéloïde aiguë ou lymphomes à cellules T), l'équilibre de cette régulation est déplacé : les cellules cancéreuses surproduisent les protéines BCL2 anti-apoptotiques, ce qui évite la mort cellulaire programmée. Ces protéines dites de «groupe de survie» sont donc des cibles d’intérêt pour l'action d’un médicament anti-cancéreux –si ces «bloqueurs d'apoptose» peuvent être piégés dans les cellules cancéreuses (sans affecter les bloqueurs d'apoptose des cellules saines) cela représente un moyen de préférentiellement « pousser au suicide» les cellules cancéreuses.
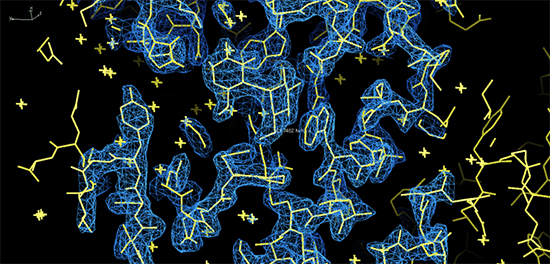
Dans le cadre de la recherche industrielle menée au synchrotron SOLEIL par achat de temps de faisceau, la société pharmaceutique britannique VERNALIS (commanditée par les groupes de recherche Servier) a obtenu sur la ligne PROXIMA-1 des résultats publiés dans la revue Nature. Cette étude, basée sur la technique de diffraction des rayons X, a fourni l'information structurelle pour aider à comprendre la fonction du candidat médicament S63845, qui se lie très fortement et spécifiquement à la protéine anti-apoptotique MCL1. MCL1 est produite dans la cellule via plusieurs voies oncogènes. Le mode de liaison de S63845 à MCL1 (voir Fig 1) imite l'action des protéines anti-apoptotiques exprimées dans les cellules saines. Les tests initiaux indiquent que S638345 possède à la fois une toxicité faible envers les cellules saines, et une efficacité élevée contre les lignées de cellules cancéreuses in vitro et in vivo. S638345 devrait ainsi empêcher spécifiquement les cellules cancéreuses d’échapper à la mort cellulaire programmée.