Des souris et des hommes… et de l’acide urique
Chez l’homme l’excès d’acide urique (ou hyperuricémie) est associé à, ou responsable de plusieurs problèmes de santé graves : syndrome métabolique1, goutte, dysfonctions des reins. Or les autres êtres vivants ne sont pas sujets à l’hyperuricémie car ils possèdent une enzyme, absente chez les hominidés, qui dégrade l’acide urique. Afin de mieux comprendre le rôle de l’acide urique dans ces pathologies, des chercheurs de l’Université de Lausanne, de l’UPMC et de l’Hôpital Tenon ont bloqué la dégradation de l’acide urique chez une lignée de souris, et en ont étudié l’impact sur leur santé, en présence ou non d’un régime alimentaire trop riche. La microscopie infrarouge de la ligne SMIS a ensuite permis d’analyser la composition des cristaux formés dans les reins des souris ne dégradant plus l’acide urique. Leurs résultats motivent à faire attention à notre alimentation…
L’acide urique est une molécule provenant de la dégradation de composés appelés purines, qui constituent notamment l’ADN, et sont apportées dans l’alimentation principalement par les viandes et poissons. Chez l’homme en bonne santé l’acide urique est éliminé dans les urines et présent en quantité modérée dans le sang (plasma).
Acide urique : avantages et inconvénients
Grâce à l’enzyme appelée urate oxydase ou uricase tous les organismes, des bactéries aux mammifères, sont capables de dégrader l’acide urique qui n’est donc pas le « déchet final » du catabolisme des purines. Tous les organismes… à l’exception des primates supérieurs, et donc des humains.
En effet au cours de l’évolution les hominidés ont perdu la capacité de produire l’uricase. Il a été proposé (sans preuve directe jusqu’alors) que l’acide urique, par son rôle de puissant antioxydant, aurait un effet protecteur sur l’organisme, avec pour conséquence d’allonger la durée de vie et de diminuer le taux de cancers liés à l’âge.
Mais l’acide urique n’a pas que des effets positifs, ce qui rend sujet à controverse l’hypothèse d’un intérêt de la perte de production de l’uricase au cours de l’évolution. En effet lorsqu’il est présent en excès (hyperuricémie), l’acide urique expose l’organisme à des problèmes de santé graves : goutte, dysfonctions rénales et (sujet fortement controversé), certains aspects du syndrome métabolique1,. Cependant l’hyperuricémie seule ne provoque pas les différents problèmes physiologiques cités.
Comprendre les effets d’un excès d’acide urique
Afin d’étudier l’influence de l’hyperuricémie sur la santé, des chercheurs ont développé un modèle animal qui, comme l’homme, ne dégrade pas l’acide urique : une lignée de souris chez laquelle l’acheminement de l’acide urique vers l’uricase est altéré, car le gène codant pour Glut9, une enzyme de transport de l’acide urique, a été inactivé dans leur foie (organe principal de production de cette enzyme).
Dans un premier temps, quatre groupes d’animaux ont été étudiés : des souris possédant ou non l’enzyme de transport, et nourries ou non avec des aliments très riches en graisse.
Chez toutes les souris déficientes Glut9, le taux sanguin d’acide urique était élevé, sans toutefois atteindre les valeurs mesurées chez l’homme. Et, à part l’obésité provoquée par le régime à l’huile de noix de coco, leur santé était bonne : pas de problème rénal.
Régime gras et excès d’acide urique, combinaison perdante
Afin de se rapprocher davantage des taux humains d’acide urique, le régime de certaines souris a été supplémenté en inosine, la molécule précurseur de l’acide urique.
Sans effet chez les souris-témoins (possédant Glut9), l’ajout d’inosine a effectivement augmenté l’uricémie des souris déficientes. Parmi elles, les animaux nourris de façon équilibrée sont rapidement revenus à la normale après quelques heures, bien qu’ils aient mangé de l’inosine pendant 3 jours. Des analyses du sang et des reins ont confirmé que, chez ces animaux, le taux d’urate sanguin a augmenté de façon transitoire sans générer de problèmes majeurs.
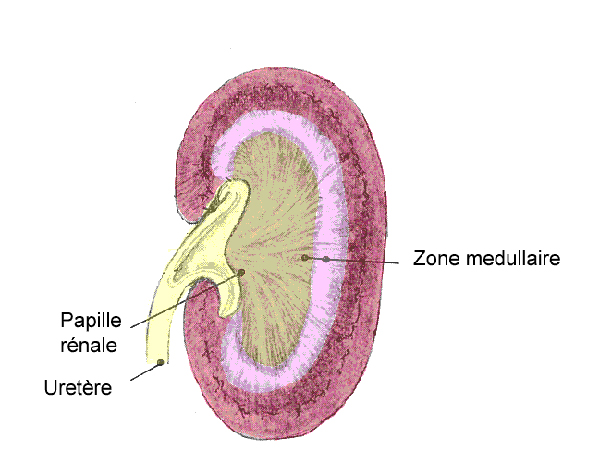
Par contre, le taux d’acide urique des souris obèses mangeant trop de graisses a augmenté à l’issue des 3 jours de consommation d’inosine : la fonction rénale des souris déficientes n’était plus correctement remplie : la formation de cristaux bloquant les tubules rénaux a empêché l’évacuation de l’urine (insuffisance rénale), et l’urate non évacué par l’urine s’est accumulé dans le sang.
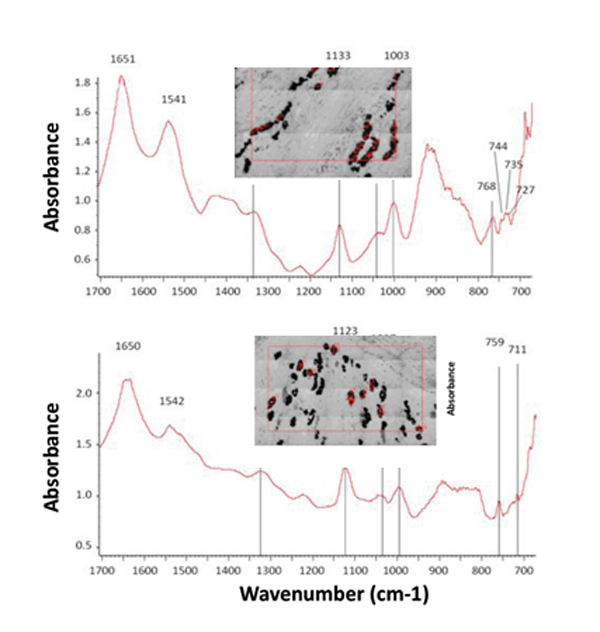
Ces cristaux, étudiés sur la ligne SMIS, étaient beaucoup plus gros et nombreux chez les souris obèses que chez les souris « à régime sain » (les souris-témoins n’avaient pas du tout de cristaux). La technique de microspectroscopie infrarouge, réalisée sur des coupes de reins, a permis de distinguer plusieurs types de cristaux, d’acide urique ou d’urate -l’ion qui provient de l’acide urique.
Pour que de tels cristaux se forment, plusieurs conditions doivent être réunies : il faut notamment que l’urine soit acide ; or l’obésité provoque l’acidification de l’urine. Ce facteur pourrait, en combinaison avec l’hyperuricémie, être à l’origine des cristaux et de la perte de la fonction rénale chez les souris sur-nourries.
Un effet réversible, mais des séquelles à long terme
Plusieurs semaines après l’arrêt de l’apport en inosine, les chercheurs ont à nouveau étudié le sang et les reins des souris. Il est apparu que, même si les animaux avaient récupéré de cette insuffisance rénale et si les cristaux avaient disparu, les lésions des tissus engendrées par ces cristaux ont entrainé des conséquences à long terme : inflammation des reins, fibrose… Ces séquelles se sont logiquement révélées beaucoup plus aigües et étendues chez les souris obèses.
Ces différents résultats chez la souris corroborent les données épidémiologiques suggérant un rôle de l’obésité sur l’impact de l’hyperuricémie.
L’acide urique est une molécule dont le rôle reste complexe et en partie méconnu, et notamment son pouvoir anti-oxydant qui, dans certaines conditions cellulaires, s’inverserait pour devenir pro-oxydant et favoriserait l’inflammation.
Les chercheurs ont réussi à obtenir un modèle animal grâce auquel, en combinant la modification génétique et les apports en inosine, il est envisageable d’étudier à long terme le rôle de l’hyperuricémie sur le développement de pathologies comme l’hypertension ou l’athérosclérose.
1 – syndrome métabolique : ensemble de pathologies (liées en partie à des facteurs génétiques mais principalement à l’environnement : activité et nutrition) qui, lorsqu’elles sont associées, augmentent le risque de développer des accidents cardiovasculaires et de développer le diabète.