Des membranes des Archées à l’industrie : la clé de la réaction de biosynthèse du mévalonate révélée
Des chercheurs de l´institut Max Planck pour la microbiologie terrestre (Marburg, Allemagne), de l’Institut de Biologie Structurale (Grenoble) et de l´ENS (Lyon) ont déterminé la structure du complexe d’enzymes responsable de la synthèse du mévalonate, brique de base constituant la membrane des Archées. De plus, ils ont compris quelle « astuce moléculaire » permet à cette réaction de se produire malgré une première étape très défavorable au point de vue énergétique. Une découverte qui intéresse aussi le domaine de l’industrie, le mévalonate étant une molécule utilisée pour la synthèse de nombreuses substances chimiques.
Les membranes lipidiques des archées sont constituées d´isoprènes qui sont produits à partir de mévalonate. La synthèse du mévalonate est coordonnée par trois enzymes : la thiolase, l´HMG-CoA synthase (HMGCS) et l´HMG-CoA réductase. La première réaction de cette synthèse, catalysée par la thiolase est très endergonique (le flux de production est très faible, la réaction nécessite un apport d’énergie pour avoir lieu) ce qui est en contradiction avec la vitesse de croissance rapide des archées, et donc de leur synthèse lipidique.
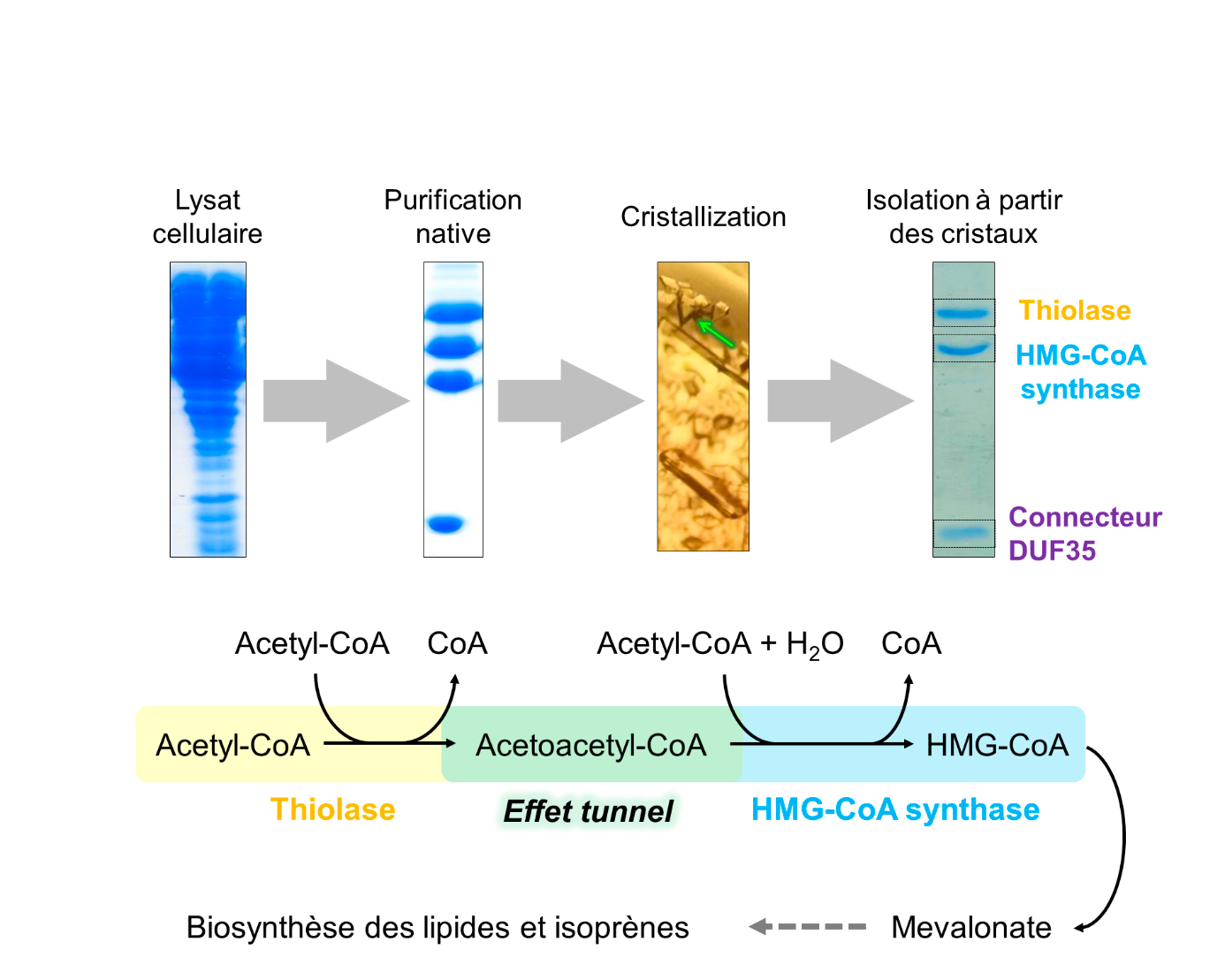
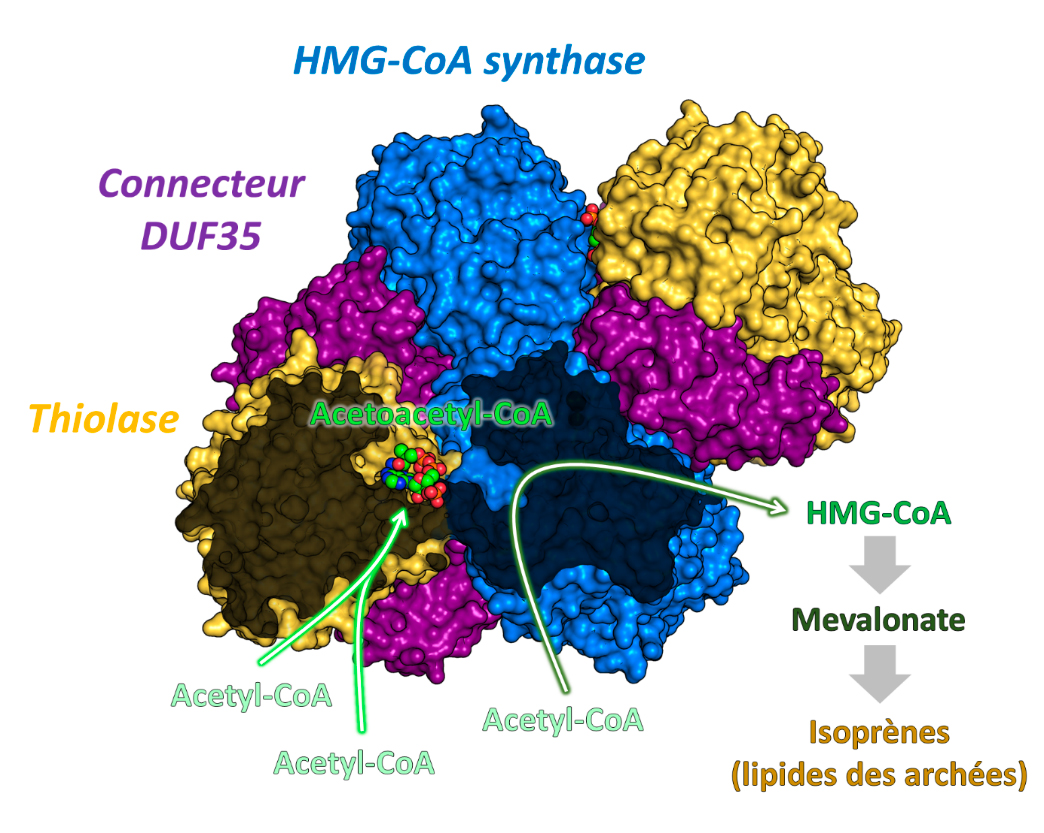
Des chercheurs de l’équipe de Seigo Shima et Tobias Erb de l´institut Max Planck pour la microbiologie terrestre à Marburg (Allemagne), en collaboration avec des chercheurs de l’équipe d’Eric Girard à l’Institut de Biologie Structurale de Grenoble et d’Olivier Maury à l´ENS de Lyon, ont joint leurs efforts pour dévoiler l´astuce moléculaire qui permet aux archées d´accélérer la vitesse de la thiolase. En purifiant la thiolase directement à partir de cellules d´archée, les chercheurs se sont aperçu que cette enzyme formait un complexe naturel avec l´HMGCS, la deuxième enzyme de la biosynthèse (Figure 1) du mévalonate. Les deux enzymes sont maintenues ensemble par une troisième petite protéine connectrice (appelée DUF35). En utilisant le Tb-Xo4, un nouvel outil induisant la cristallisation et facilitant fortement la détermination structurale (présence d'un atome de lanthanide), et la technique de diffraction de rayons-X de cristaux de protéines sur la ligne de lumière PROXIMA-2A, la structure du complexe protéique thiolase/HMGCS/DUF35 a été résolue (Figure 2).
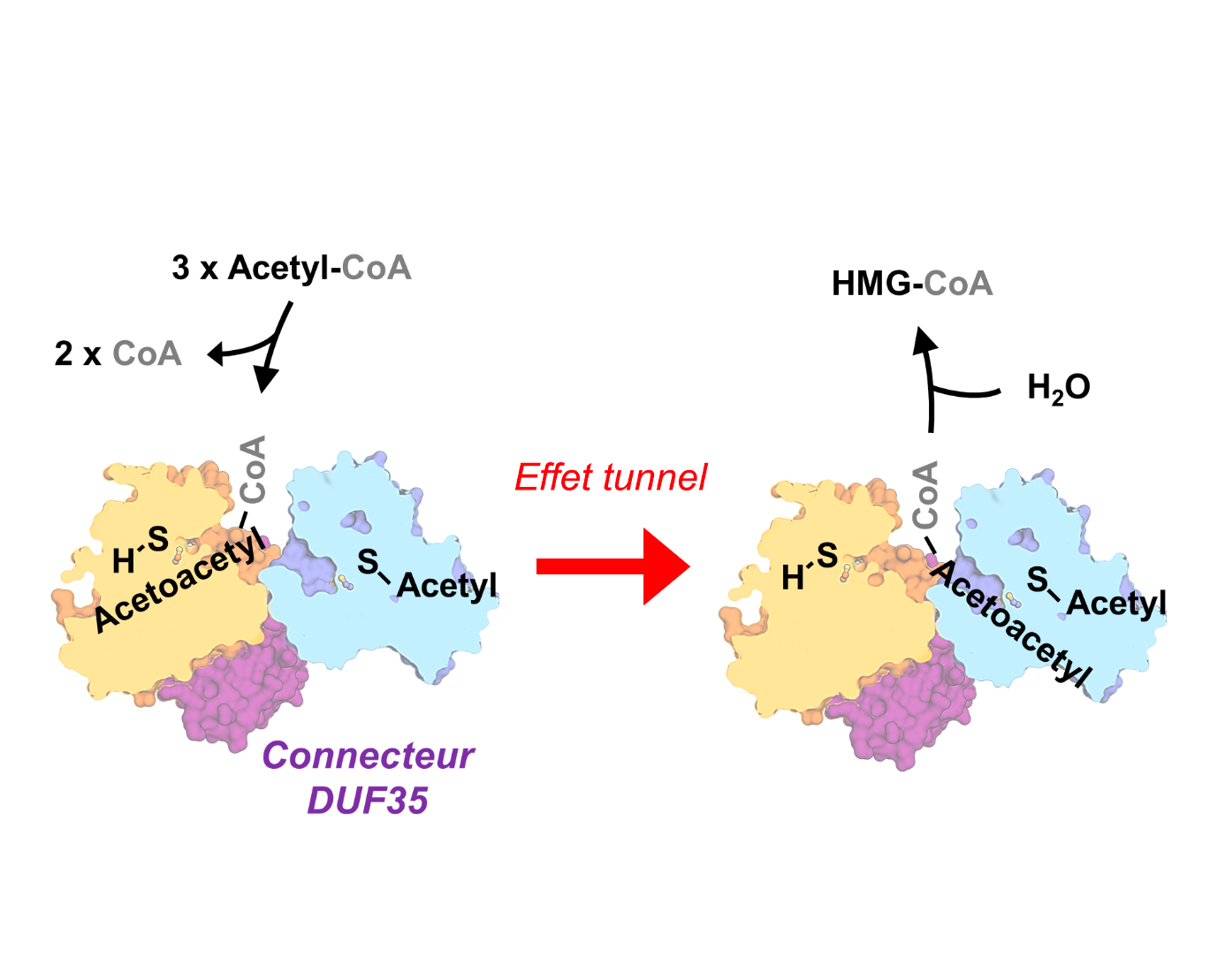
L´étude structurale et biochimique a révélé la clé de la réaction : la thiolase et l´HMGCS utilisent le même site de fixation pour leur substrat, l’AcetylCoA. Ce site unique permet un « effet tunnel » qui déplace favorablement la réaction et augmente ainsi considérablement la vitesse de synthèse. En d´autres termes, la réaction endergonique de la thiolase est tractée par la réaction exergonique (elle fournit de l’énergie) de l´HMGCS (Figure 3).
Cette découverte est de première importance pour l´industrie : le mévalonate est une molécule précurseur qui permet la synthèse de nombreuses substances chimiques, comme les caoutchoucs synthétiques.