Contamination des eaux - la calcite peut-elle piéger l’arsenic ?
La contamination des eaux souterraines par l'arsenic (As) constitue une menace environnementale grave pour la santé dans de nombreux pays du monde. Comprendre le mécanisme d'absorption et de libération de l’arsenic par les minéraux peut aider à établir des stratégies de décontamination. Mais des matériaux comme la calcite, omniprésente dans la croûte terrestre, sont difficiles à étudier du fait de leur structure complexe et inhomogène. La technique de microspectroscopie d'absorption des rayons X sur synchrotron apparaît alors comme un outil de choix.
Le poison arsenic
L'arsenic est un élément semi-métallique du tableau périodique. Il est inodore et sans goût, et pénètre dans le réseau d'approvisionnement en eau potable depuis des dépôts naturels dans le sol ou par certaines pratiques agricoles ou industrielles. Lorsque de l'eau souterraine contaminée par de l'arsenic est utilisée comme eau potable, elle constitue un danger pour la santé des consommateurs. Une exposition prolongée à l'arsenic peut avoir divers effets tels qu'un épaississement et une décoloration de la peau, des douleurs d'estomac, des nausées, des vomissements, des diarrhées, un engourdissement des mains et des pieds, une paralysie partielle ou encore une cécité. L'arsenic est aussi considéré comme cancérigène et a été associé à des cancers de la vessie, des poumons, de la peau, des reins, des voies nasales, du foie et de la prostate.
La source principale de contamination n'est pas anthropique mais géologique, c'est-à-dire due à une érosion ou une dissolution de minéraux de roche porteurs d'arsenic, suivie de la libération de quantités d'arsenic pouvant atteindre des milliers de mg/L (la concentration maximale admissible définie par l'agence américaine pour la protection de l'environnement (EPA) étant de 0,01 mg/L). Par conséquent, il est important de localiser les eaux souterraines riches en arsenic afin d'agir pour éviter des problèmes de santé chez les populations locales. L'Asie du Sud-Est est la région la plus gravement touchée par la contamination naturelle à l'arsenic dans les eaux souterraines, avec une situation particulièrement grave au Bangladesh, au Népal, au Vietnam et en Chine. Toutefois, l'Europe comporte aussi des territoires avec des eaux souterraines fortement enrichies en As, mais à une échelle plus régionale.
Des eaux souterraines hautement contaminées à l'arsenic ont été découvertes dans le bassin pannonien (Hongrie, Roumanie, Croatie et Serbie) mais aussi en Espagne, en Italie, en Grèce et en France (par exemple dans la région de Cézallier du Massif central : voir réf. 1). De nombreux pays européens ne disposent pas de rapports sur la situation de l'arsenic dans les eaux souterraines.
Comment étudier le piégeage de l’arsenic par les minéraux
Au-delà de la localisation des zones à risque, il est aussi capital de comprendre le mécanisme d'absorption et de libération de l’arsenic par les minéraux de roche, car de telles informations peuvent aider à établir des stratégies de décontamination. De nombreux minéraux naturels ou artificiels peuvent absorber des quantités considérables d'arsenic. En raison de l'omniprésence de ce minéral dans la croûte terrestre ainsi que de sa stabilité dans divers environnements géologiques, la calcite (CaCO3) peut jouer un rôle important pour limiter la mobilité de l'arsenic.
Bien que plusieurs études aient été effectuées sur la calcite synthétique, l'efficacité de la calcite naturelle en tant que piège minéralogique de l’arsenic n'a pas été étudiée en détail, notamment en raison des difficultés intrinsèques pour travailler avec des matrices complexes et inhomogènes. Dans ce domaine, les techniques utilisant le rayonnement synchrotron ont prouvé leur grande utilité. En particulier, des cartes haute résolution de distribution des éléments peuvent révéler l'association de As avec d'autres phases minérales présentes dans les échantillons naturels de calcite (principalement des oxyhydroxydes de Fe et Mn), tandis que la microspectroscopie d'absorption des rayons X (XAS) révèle l'état d'oxydation de As en des points d'intérêt déterminés à partir des cartes de distribution des éléments.
L’intérêt de la microspectroscopie d'absorption des rayons X
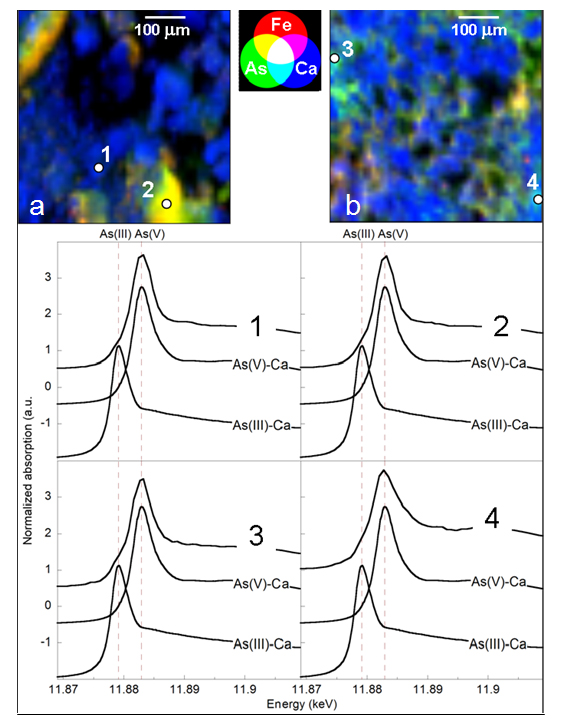
Des fragments d'échantillons naturels de calcite, tels que des travertins lacustres riches en As de la vallée de la rivière de Pecora (Italie), ont été préparés en sections fines polies et étudiés sur la ligne de lumière DiffAbs en acquérant plusieurs cartes de distribution des éléments sur 500x500 µm à des résolutions de 10 µm (Figure 1, partie supérieure). En outre, plusieurs spectres XANES (spectroscopie de structure près du front d'absorption de rayons X) ont été acquis en des points d'intérêt sur ces cartes (Figure 1, partie inférieure). Les résultats de cette étude confirment les résultats obtenus précédemment (réf. 2,3,4) à l'aide de la méthode XAS (sur synchrotron) dans le volume d’échantillons, ainsi que par d'autres techniques. En particulier, cette expérience a permis de confirmer que dans les travertins naturels étudiés, As(III) était incorporé dans le réseau de calcite par le mécanisme de substitution arsénite-carbonate suggéré par Román-Ross et al. (réf.5). Toutefois, cette substitution ne se produit que pour une faible fraction de la quantité totale de As présente dans ces travertins. L'incorporation par la calcite est susceptible de devenir importante dans les milieux ne favorisant pas l'adsorption de As sur des oxyhydroxydes de Fe (par exemple dans les environnements réducteurs et/ou alcalins). Ceci peut avoir une forte incidence en termes d'environnement, car quand As est incorporé dans une phase minérale -au lieu d’être adsorbé à la surface du minéral- l’arsenic est beaucoup moins disponible dans l'environnement.
Références :
1. Le Guern C. et al (2003) Appl. Geochem. 18, 1313–1323.
2. Di Benedetto F. et al. (2006) Earth Planet. Sci. Lett. 246, 458–465.
3. Costagliola P. et al. (2007) IMWA Symposium 2007: May 27–31 (eds. F. Frau and R. Cidu), Cagliari/Sardinia Italy, pp. 415–418.
4. Bardelli F. et al. (2011) Geochim. Cosmochim. Acta 75, 3011–3023.
5. Román-Ross G. et al. (2006) Chem. Geol. 233, 328–336.