Casser des molécules avec un rayonnement UV : une nouvelle méthode d’activation pour la spectrométrie de masse tandem
La spectrométrie de masse en tandem tient une place centrale en chimie analytique et structurale. Cette technologie consiste à casser les molécules étudiées pour, en analysant leur façon de se fragmenter, déduire des informations sur leur structure initiale.
De la méthode employée pour cette fragmentation va dépendre la qualité du contenu informatif obtenu. L’un des outils permettant de briser des liaisons chimiques des molécules est la lumière. En collaboration avec l’INRA, un scientifique de SOLEIL a identifié une portion du spectre électromagnétique particulièrement efficace pour réaliser la fragmentation des molécules, et mis au point une nouvelle source de fragmentation des molécules pour la spectrométrie de masse.
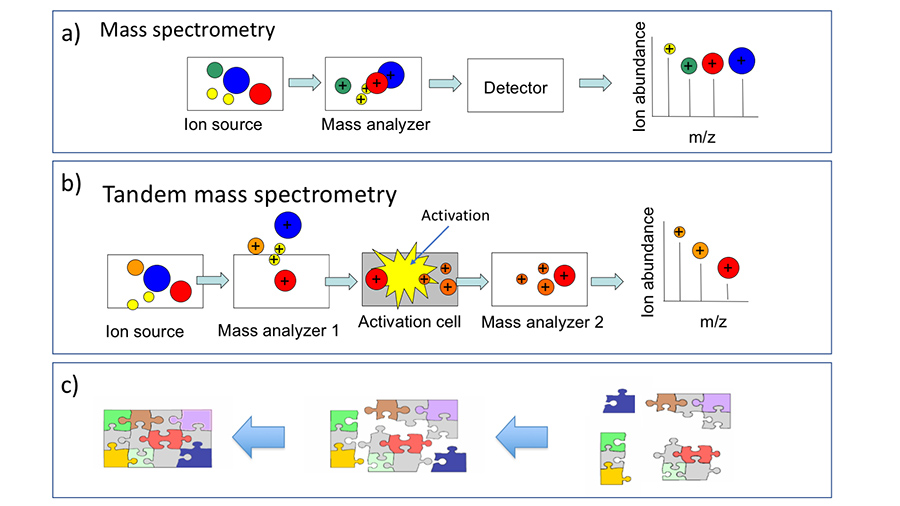
Depuis l’avènement des méthodes ’modernes’ d’ionisation (comme par exemple l’électrospray et le MALDI), la spectrométrie de masse est devenue une technologie centrale en sciences analytiques. Un spectromètre de masse est composé de (figure 1 a) :
- une source d’ionisation capable de placer des molécules en phase gazeuse et de leur conférer une charge électrique,
- un analyseur de masse, qui sépare les ions selon leur rapport masse sur charge (m/z),
- un détecteur qui enregistre le passage des ions, en fonction de m/z.
Un spectre de masse est une représentation de l’abondance des ions en fonction de leur rapport m/z. A partir de la mesure de ces rapports m/z il est notamment possible de calculer la masse molaire des espèces étudiées.
Il existe une variante de la spectrométrie de masse « simple », qui donne plus d’informations que cette dernière. En effet, l’ajout d’une étape supplémentaire de filtrage en masse, comme représenté à la figure 1 b), permet d’isoler l’un des ions obtenus lors de la 1è étape, de lui faire absorber de l’énergie (on parle d’étape d’activation) et d’observer les ions-fragments qui résultent de cette absorption d’énergie.
Cette méthode est appelée spectrométrie de masse tandem, MS/MS ou encore MS2. Lorsqu’on effectue successivement plusieurs étapes de sélection et d’activation, on parle de MSn.
L’intérêt de la MS/MS est de pouvoir remonter à la structure de l’ion précurseur à partir de l’analyse des profils de fragmentation, comme illustré à la figure 1 c).
Cette technique est aujourd’hui largement utilisée pour le séquençage des macromolécules biologiques (protéines, etc.).
Comment améliorer l’étape d’activation ?
En spectrométrie de masse tandem, l’étape d’activation des ions est cruciale car elle détermine pour une large part la nature des produits de fragmentation. La méthode la plus employée est appelée « dissociation induite par collision » (collision induced dissociation, CID). Elle consiste à provoquer des collisions inélastiques entre les ions étudiés et un gaz inerte (par exemple N2 ou Ar) dans une cellule de collision.
La CID, proposée par défaut dans tous les appareils commerciaux de MS/MS, revient à appliquer un chauffage lent aux ions. Les multiples collisions subies par les ions augmentent progressivement leur énergie interne jusqu’à atteindre un seuil de dissociation. En conséquence, les liaisons les plus faibles sont brisées. Or, ce n’est pas toujours souhaitable, notamment lorsque les espèces d’intérêt possèdent des groupes chimiques labiles comme les modifications post-traductionnelles des protéines (phosphorylations ou glycosylations), ou dans le cas d’assemblages fragiles tels que les complexes non covalents formés entre les molécules biologiques et leurs ligands. A la moindre activation par CID ces complexes se dissocient, et l’information sur la localisation des sites d’interaction molécule/ligand, d’une importance capitale dans de nombreux domaines (mode d’action des drogues, reconnaissance moléculaire…), est perdue.
Malgré la facilité de mise en œuvre et le coût relativement bas de la CID, ces limitations ont motivé le développement de méthodes alternatives.
La solution : de la lumière
Une façon de fournir beaucoup d’énergie rapidement à un ion est de lui faire absorber des photons. Plus les photons seront énergétiques, plus la quantité d’énergie fournie sera importante. Cette idée a été mise en œuvre à travers le couplage de lasers puissants, émettant dans les domaines de l’ultraviolet (UV) et l’ultraviolet du vide (VUV), avec des pièges à ions. L’activation d’ions par irradiation UV ou VUV possède des caractéristiques spécifiques qui sont complémentaires d’autres méthodes d’activation comme la CID.
Néanmoins, les longueurs d’onde d’émission laser sont limitées : les lasers commerciaux permettent d’accéder uniquement aux états électroniques excités de plus basse énergie. La question de l’utilisation de rayonnements plus énergétiques se pose alors naturellement.
Afin d’explorer la région des plus hautes énergies, un spectromètre de masse de type de piège à ions a été successivement couplé avec les lignes de lumière DISCO et DESIRS. En effet, le rayonnement synchrotron est une source brillante et accordable (possibilité de choisir une longueur d’onde –ou énergie- donnée) sur une très grande gamme d’énergies. Cela permet d’explorer les fragmentations induites par l’absorption de lumière sur l’ensemble du spectre électromagnétique.
Les principales familles de molécules biologiques ont pu être étudiées : sucres, protéines, etc, et de nouvelles voies de fragmentations ont été mises en évidence.
Ainsi, il est apparu que la gamme d’énergie la plus efficace pour la spectrométrie de masse tandem se situe autour de 20 eV (~60 nm de longueur d’onde) dans une région appelée extrême ultraviolet (XUV). En effet, ce domaine correspond au maximum de l’absorption de la plupart des espèces chimiques et elle produit un régime particulier de fragmentation appelé photoionisation dissociative (DPI en anglais).
Or, il se trouve que cette gamme de longueurs d’onde, bien qu’inaccessible aux lasers commerciaux, est à la portée des lampes à décharge.
Du synchrotron vers le laboratoire
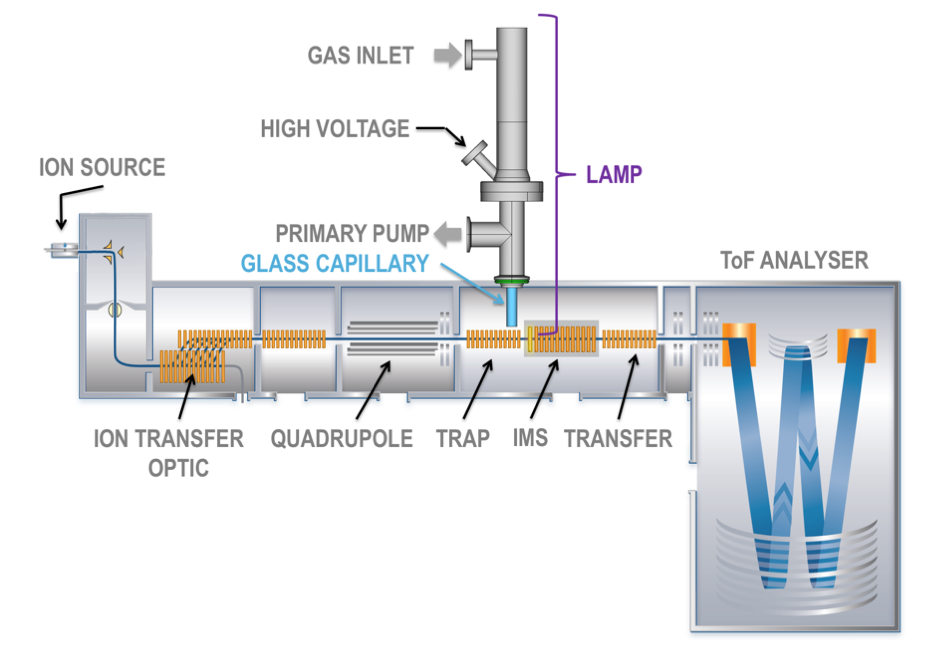
Un scientifique de la ligne DISCO, également affilié à l’INRA, s’est basé sur les résultats obtenus avec la lumière de SOLEIL pour concevoir et installer une lampe à décharge sur un spectromètre de masse commercial. Le système a été testé avec succès sur des molécules modèles (sucres, peptides, etc). Les fragmentations induites par le rayonnement issu de la lampe – la décharge dans l’hélium s’est révélé être la plus efficace – reproduisent les observations faites en utilisant le rayonnement synchrotron.
Une nouvelle méthode d’activation pour la spectrométrie de masse tandem, basée sur un rayonnement XUV produit par une décharge dans un gaz rare, a ainsi été développée.
Cette technologie met donc en œuvre des rayonnements qui sont capables de photoioniser des ions produits par électrospray ou par MALDI, afin de provoquer leur fragmentation. Les profils de fragmentation obtenus sont complémentaires des autres méthodes et, dans certains cas, les contenus informatifs sont de meilleure qualité.
Cette méthode peu coûteuse et facile à installer sur un équipement commercial n’est pas soumise aux contraintes de sécurité imposées aux lasers. Elle vient donc compléter avantageusement l’arsenal des méthodes d’activation dont disposent les scientifiques.