La structure et le pouvoir nutritif des cristaux de lait de cafard
Un travail de recherche sur la génération de cristaux naturels de protéines par une espèce vivipare de cafards a été effectué en partie sur la ligne PROXIMA-1.
Suivant un mode de recherche « à l'ancienne », tout a débuté par un simple geste de curiosité quand en Iowa (USA), le jeune chercheur Nathan Coussens fut intrigué par des objets cristallins brillants extraits d'insectes. C'était il y a environ 10 ans. Le sujet a depuis fait son chemin, et c'est dans un esprit collaboratif international regroupant des équipes américaines, indiennes, canadiennes, japonaise et française (PROXIMA-1) que le mystère sur ces cristaux a pu être levé.
Les cristaux proviennent de la substance nutritive secrétée par les femelles cafard pour le développement et la croissance de leur progéniture. Ce "lait" se transforme naturellement en cristaux dans l'intestin des "nourrissons", constituant un stock qui se libère en fonction des besoins nutritifs du petit.
Afin de comprendre la composition à l'échelle atomique de ces cristaux contenant à la fois des protéines, des lipides et des sucres (soit un aliment complet), les chercheurs en ont déterminé la structure 3D par diffraction de rayons X sur la ligne de lumière PROXIMA-1. Malgré la composition complexe et hétérogène de cette substance nutritive, les cristaux formés in vivo sont stables et diffractent remarquablement bien.
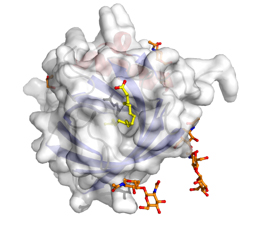
Ils sont très énergétiques (trois fois plus que la même quantité de lait de vache) et les rayons X révèlent que la libération prolongée de leurs constituants provient de la structure en forme de "baril" de la partie protéique, qui enserre une molécule de lipide.
Le sujet, qui démarra par un simple acte de curiosité, devient aujourd'hui un projet de recherche à part entière à SOLEIL. Dans ce programme, les membres de l'équipe PROXIMA-1 sont plus particulièrement intéressés par l'étude des modes naturels de cristallisation. La résolution de ces structures de cristaux synthétisés in vivo par les cafards est une première étape et ouvre la porte à l'étude de bien d'autres exemples de cristaux issus du vivant encore plus exotiques.