Dommages causés par les rayons X dans les systèmes biologiques : identifier les électrons émis après irradiation par rayons X
Comprendre les mécanismes des dommages causés par les rayons X dans les systèmes biologiques est d'un intérêt primordial en médecine (radioprotection, radiothérapie...). Les rayons X mous, d'une énergie comprise entre 100 et 1000 eV, peuvent arracher des électrons fortement liés aux atomes constituant la matière organique – c’est le phénomène d’ionisation. Cette ionisation est suivie de l'émission d'un 2è électron (« électron Auger »). Or, en solution, ces deux électrons libérés peuvent induire des dommages. Est-on capable d'identifier ces électrons émis, et leur histoire ?
Pour répondre à cette question, une équipe du LCP-MR (Paris) a conçu un spectromètre d'électrons par temps de vol à bouteille magnétique, qui a été couplé au micro-jet liquide présent sur la ligne de lumière PLEIADES. Des mesures dites en coïncidences ont permis de distinguer les conséquences de l'ionisation de deux atomes de carbone ayant un environnement chimique différent.
L'exposition d'une molécule à un rayonnement ionisant tel que les rayons X induit l'émission d'un électron, provenant des couches électroniques centrales des atomes, appelé photoélectron (e-ph). La molécule laissée dans un état excité (avec un "trou" dans la couche électronique interne) peut alors « relaxer » par l'émission d'un second électron, l'électron Auger (e-Auger). Ces processus ultra-rapides se produisent dans la gamme des femtosecondes (10-15s) après l'interaction avec le photon X. La spectroscopie électronique, qui permet d'analyser l'énergie cinétique des électrons émis, est un outil de choix pour étudier ces phénomènes. Néanmoins, même pour des molécules isolées (gaz), les spectres d'électrons Auger sont difficiles à interpréter en raison des nombreuses voies de désexcitation produites par chaque photoélectron. En milieu liquide, des interactions supplémentaires induites par le solvant compliquent encore l'analyse des spectres mesurés.
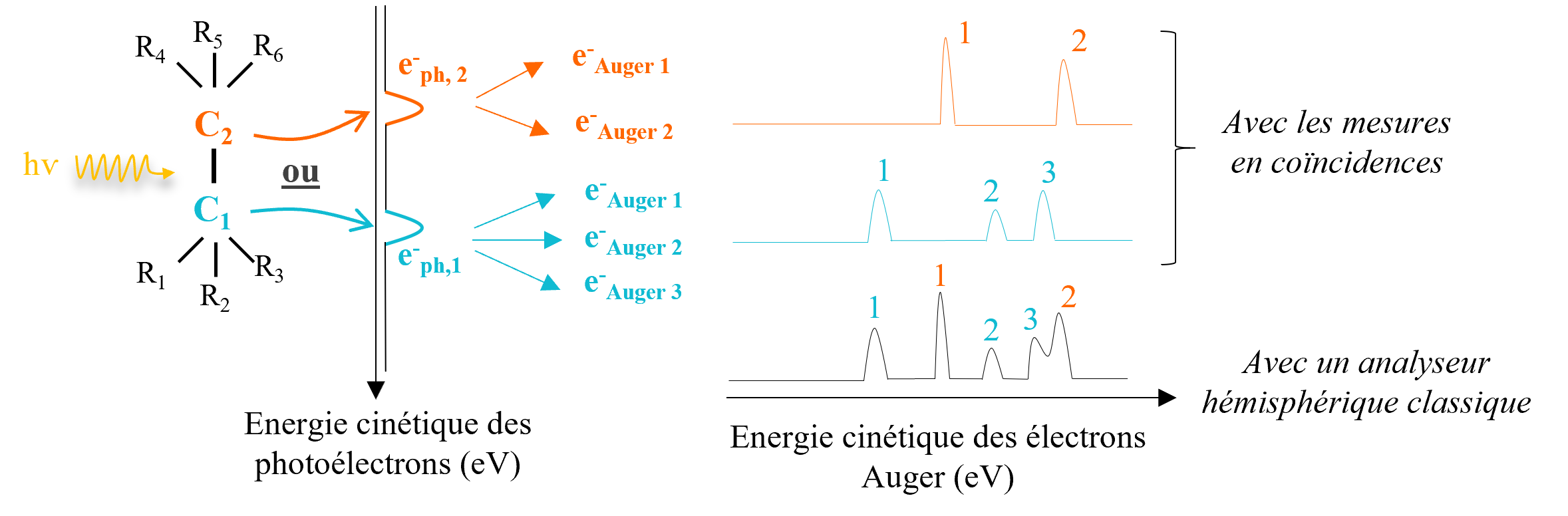
Pour favoriser la compréhension et par conséquent la distinction de chaque processus, deux conditions doivent être remplies. La première est d’arriver à identifier de façon claire la contribution des électrons du solvant et celle des électrons de la molécule en solution. La seconde est la distinction entre les différents processus Auger qui ont eu lieu suite à l'ionisation de plusieurs atomes au sein d'une même molécule. La méthode des mesures en coïncidences, dont le principe est représenté schématiquement sur la Figure 1, est particulièrement adaptée puisqu'elle permet de retrouver les paires d'électrons (ici e-ph / e-Auger) issues d'un même événement d'ionisation. Comme décrit sur la Figure 1, cette méthode donne accès à des spectres Auger filtrés selon une gamme d'énergie cinétique, ce que ne permet pas une mesure classique de spectroscopie électronique.
Expérimentalement, les mesures en coïncidences réalisées avec le spectromètre d’électrons doivent être réalisées avec un mode spécial de fonctionnement temporel du synchrotron appelé mono-paquet ("single bunch"), c’est-à-dire qu’un paquet unique de particules circule dans une partie de l’accélérateur, produisant un flash unique de rayonnement. L'horloge du synchrotron, calée sur ce flash, déclenche les mesures du temps de vol des électrons vers le détecteur. Ce temps est directement lié à l'énergie cinétique des électrons.
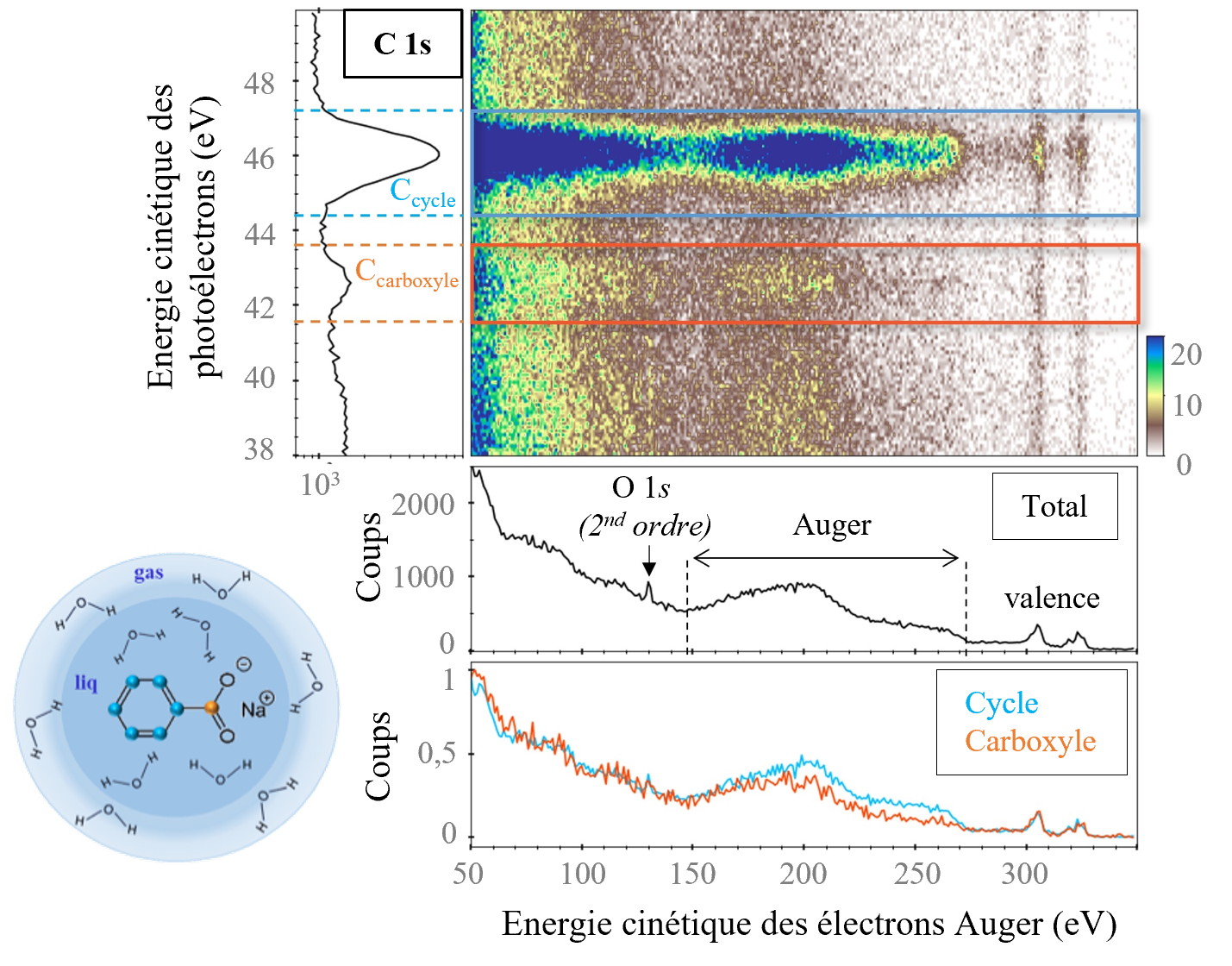
L'application de cette technique à un échantillon liquide implique la mise en œuvre d'un dispositif de micro-jet liquide. Les équipes de scientifiques ont combiné ces deux techniques pour étudier les molécules de benzoate de sodium solvatées dans l'eau, représentées schématiquement dans le micro-jet dans la Figure 2. Le benzoate de sodium est composé de deux groupements chimiques différents : le cycle aromatique dont les carbones sont identifiés par des sphères bleues et le groupement carboxyle dont le carbone est identifié par une sphère orange. Sur la ligne PLEIADES, les mesures ont été effectuées en utilisant des rayons X d’énergie supérieure au seuil de la couche électronique 1s de l’élément carbone. Les résultats obtenus sont présentés dans la Figure 2.
En raison de la présence de deux environnements chimiques différents pour le carbone, deux pics sur le spectre de photoélectrons sont identifiables (spectre à gauche). Comme dans la Figure 1, deux spectres Auger filtrés sur la gamme d'énergie des photoélectrons ont été obtenus (spectres sous la cartographie 2D).
Les différences observées entre ces deux spectres peuvent être considérées comme une illustration concrète de l'intérêt des mesures par coïncidences. Des calculs théoriques sont nécessaires pour expliquer ces différences.
Ces résultats encourageants permettront de déterminer les distributions d'énergie des électrons émis dans un liquide au sein duquel ils peuvent causer des dommages. Ils serviront ainsi de données pour des simulations. Cette méthode permet également de sonder les transferts d'énergie entre le soluté et la solution.